

在确保临床试验数据可靠性、过程合规性与受试者安全性的多重保障机制中,稽查(Audit)构成了超越日常监查的、更深层级的质量审视与验证防线。它并非对常规工作的简单重复检查,而是一项具有特定哲学、严格标准与独立视角的系统性评估活动。对于致力于构建高质量研究管理体系的临床试验机构而言,深刻理解稽查的本质、价值与要求,是提升自身稳健性、赢得广泛信任并实现长远发展的关键认知。一、稽查的核

在药物临床试验的质量链条中,试验用药品的管理是贯穿始终、风险高度集中的关键环节。其管理质量直接关系到受试者用药安全、疗效评估的科学性以及整个研究的合规根基。根据《药物临床试验质量管理规范》(GCP)的明确规定,对试验用药品的供应、储存、分发、收回及记录的全面核实,是监查员的核心职责之一。对于临床试验机构而言,深入理解这一监查重点,并以此为导向构建超越基本合规的、体系化的内部管理
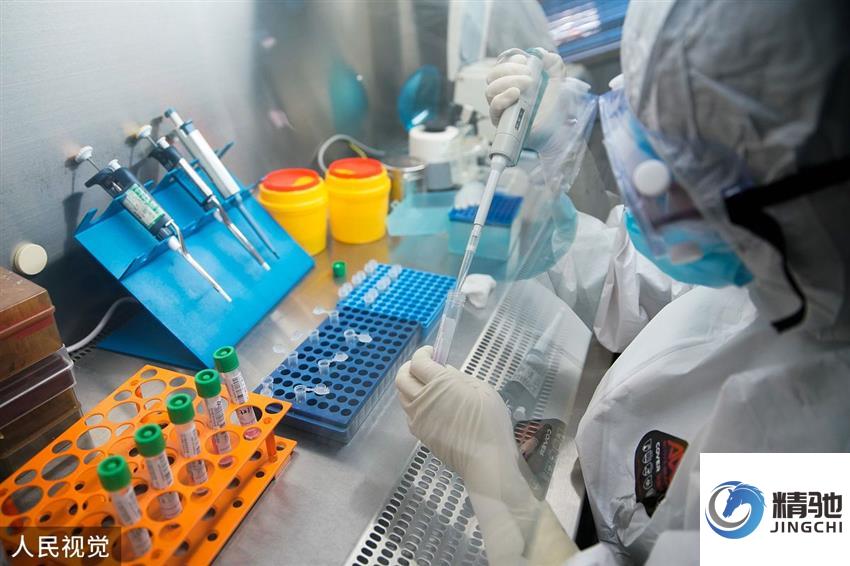
临床试验监查是保障研究质量、保护受试者权益的核心监督机制,其复杂性与系统性远超简单的现场检查。它是由申办者主导、贯穿试验全程、融合多元策略的动态质量管理过程。对于承担试验执行的医疗机构而言,深入理解监查的法规要求与科学内涵,不仅是“被动接受检查”,更是“主动参与共建质量体系”的起点。构建一个能够与高效监查体系顺畅互动、协作的内部管理体系,是临床试验机构专业化与成熟度的关键标志。

在药物临床试验中,受试者对研究方案的遵从程度,即用药依从性,是影响研究结果科学性与可靠性的关键因素。理想的疗效与安全性数据建立在假定受试者按方案规定用药的基础上。因此,准确评估、有效管理和科学分析用药依从性,不仅是评价研究质量的必要环节,更是解读试验结果、做出合理推断的基础。系统化的依从性管理能力,是现代临床试验机构专业性的重要体现。一、依从性评估的核心:量化计算与多维验证1.

在药物临床试验的动态管理过程中,并非所有入组的受试者都能最终完成预设的全程访视与治疗。明确区分“剔除”与“脱落”两种不同的退出情况,并规范其判定、记录与处理流程,是保障研究科学性、数据分析完整性以及伦理合规性的基础环节。这两个概念的核心差异在于退出决策的主动发起方不同,这直接影响了该受试者数据在统计分析集中的归属,也反映了研究管理的不同侧面。一、概念核心辨析:决策权归属与退出原

在药物临床试验的执行层面,一支高效、专业的研究团队是保障试验质量与进度的核心。其中,研究护士与临床研究协调员是研究者在现场最重要的两位协助者。尽管他们的工作存在交集,且共同服务于试验的顺利开展,但其角色定位、核心职责与专业背景存在本质区别。清晰界定两者的分工与协作界面,对于优化团队效能、明确责任边界、确保研究合规至关重要。一、核心角色定位:护理专业与项目协调1. 研究护士:临床

随着信息技术在临床研究中的深度应用,电子数据与电子文件已成为现代临床试验的核心资产。其保管的可靠性、安全性与可溯源性,直接决定了研究数据的完整性、可审核性及最终注册申报材料的有效性。“刻盘保管”仅是长期存档的一种物理形式,而完整的电子文件管理是一套涵盖生成、存储、备份、归档、检索及销毁的全生命周期合规体系。构建这套体系,是临床试验机构迈向信息化、规范化管理的关键一步。一、电子文

药物临床试验的根本价值在于其产生的科学数据的真实、准确与完整。数据的真实性不仅关乎单个研究项目的成败,更直接影响药品审评决策的科学性、公众用药安全及医疗研究的公信力。确保数据真实性绝非单一环节的任务,而是贯穿研究全流程、涉及多维度、需要系统性构建的严谨工程。当前监管核查的核心,正是围绕以下六大关键领域,深入验证数据链条的坚实可靠。一、受试者筛选与入组:可溯源的身份与资格证据链受

在药物临床试验的复杂生态系统中,清晰界定各方参与者的角色、职责与立场,是确保研究高效、合规运行的基础。其中,临床研究协调员与临床监查员作为研究现场最活跃的两类专业人员,其服务主体与核心职责常被混淆。准确理解其代表方与工作边界,对于构建顺畅的研究者-申办者协作关系至关重要。一、核心角色定位:代表方与根本职责1. 临床研究协调员:研究者的专业助手与项目执行官代表方:研究者/临床试验

在临床试验的起始环节,知情同意不仅是法律与伦理的强制性要求,更是建立研究者与受试者之间信任关系的基石。这一过程的重要性,决定了其执行细节必须在医疗原始记录中得到准确、完整且规范的记载。记录本身并非目的,而是为了构建一条清晰、可追溯的审计轨迹,证明受试者是在充分理解、完全自愿的前提下参与研究,其权益在程序上得到了根本性保障。对于临床试验机构而言,这是展现其研究操作规范性与伦理严谨