

在医疗行业快速变革的今天,许多医院管理者经常思考一个问题:医院到底有没有必要投入精力去备案国家药物及医疗器械临床试验机构(GCP)资质?这项工作耗时、耗力,看起来似乎不是医院的“刚需”,那么它究竟值不值得做?带着这个问题,我们走访了多家已经完成备案的医院,也研究了国家政策走向和行业发展趋势。结论很清晰:对于谋求长远发展的医院而言,GCP资质备案不仅有必要,而且是越早布局越主动的
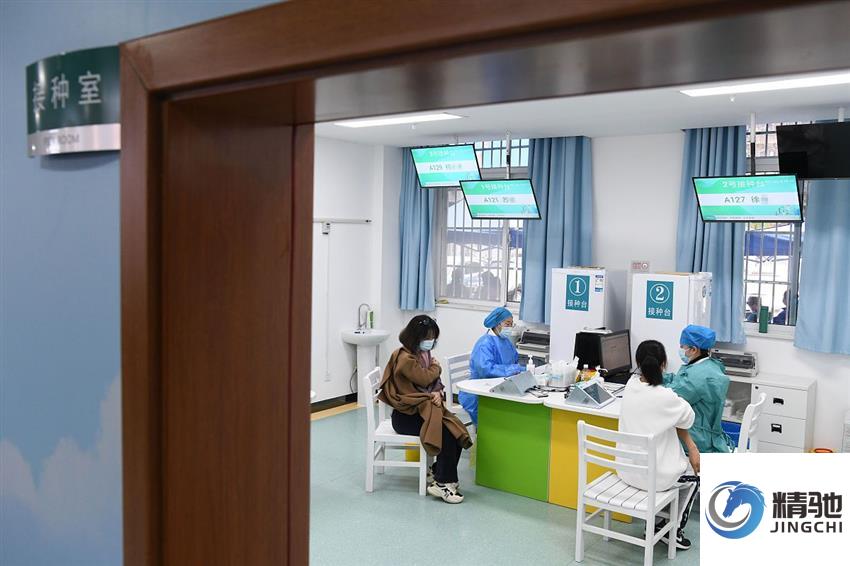
在医学科技日新月异的今天,新药研发、器械创新正在以前所未有的速度改变着临床诊疗的格局。然而,任何一项创新成果从实验室走向病床,都离不开一个关键环节——临床试验。而承担临床试验的医疗机构,必须具备国家认可的资质。这就是为什么越来越多的医院正在积极备案国家药物及医疗器械临床试验机构(GCP)资质。这一资质对于医院意味着什么?它对医学发展又有着怎样的深远意义?本文将为您系统梳理。一、

2026年是“十五五”开局之年,对于中国医疗机构而言,这不仅是一个时间节点的更替,更是发展逻辑深刻变革的关键时期。在国家卫生健康委近期召开的2026年全国医政工作会议上,“稳中求进、提质增效”被确立为全年工作的总基调。面对新形势,医院管理者们普遍在思考:新的一年,医院应当向哪些方向发力?哪些能力建设能够真正推动医院实现高质量发展?我们将从政策导向、行业趋势和医院内生需求三个维度
亲爱的合作伙伴、各位医疗同仁:新春的烟火渐渐远去,节日的余温仍在心间萦绕,但奋斗的号角已经再次吹响。在此,北京精驰医疗科技有限公司全体员工向您致以最诚挚的问候:年过完了,咱们该撸起袖子加油干了!开工大吉,我们已整装待发正月初八过后,精驰医疗的办公室里已经恢复了往日的忙碌。技术团队的同事们正在梳理节前积压的需求,项目组的伙伴们已经开始对接新一年的辅导计划,培训中心的同事们也在紧锣

对于众多计划申报国家药物及医疗器械临床试验机构(GCP)资质的医院而言,全面、客观地认识此项工作的复杂性与挑战性,是制定成功策略的首要前提。备案过程绝非简单的行政申报,而是一项涉及战略、管理、技术、资源与合规等多维度的系统性重构工程。本文旨在客观剖析医院独立完成备案所面临的实际困难,并探讨在专业化支持下实现高效、稳健推进的可行性路径。一、备案工作的系统性复杂度与多维挑战成功备案

在当今中国医疗卫生事业发展的宏观图景中,获得国家药物及医疗器械临床试验机构(GCP)资质,已从一个可选的科研能力标签,转变为众多医院,尤其是二级甲等及以上医院谋求长远发展的战略必需品。这一转变并非偶然,而是深刻植根于国家政策导向、医药产业演进、医院自身发展逻辑与医疗卫生体系现代化的多维交汇之中。一、政策环境的根本性驱动:从“鼓励”到“融合”近年来,国家层面连续出台的系列政策,清

在药物与医疗器械从构想走向患者的宏大乐章中,临床试验是一场需要精密配合的交响乐。其中,两个关键角色共同决定了演出的成败:申办方与合同研究组织(CRO)。理解他们本质的区别与协同逻辑,对于医院——这场演出中至关重要的“演出场地”与“乐手”聚集地——而言,是明确自身价值定位、构建高效合作模式、从而吸引优质“演出项目”的战略前提。一、角色本质:责任主体与服务专家从法规与商业本质上,二
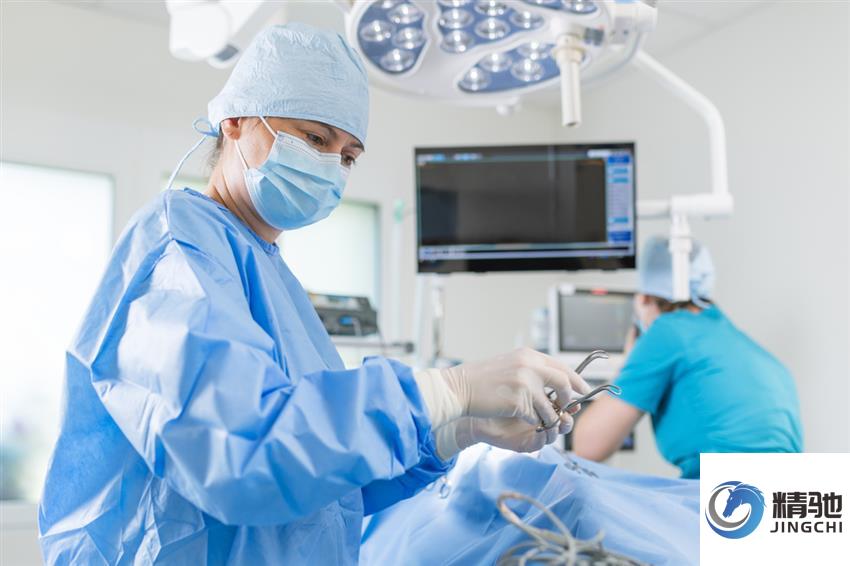
在我国医药创新体系从“仿制为主”向“创仿结合”并日益强调自主创新的战略转型期,临床研究能力已成为衡量医疗机构核心竞争力的关键指标之一。是否申请国家药物及医疗器械临床试验机构(GCP)资质,并非一个简单的行政决策,而是一项涉及医院长远发展的战略性考量。本文将系统剖析决定医院是否需要启动此项备案规划的多维因素,为医疗机构的管理层提供清晰的决策参考。一、驱动备案决策的核心政策与行业背

现场检查的结束,标志着临床试验机构备案工作进入一个以文书呈现与系统反思为核心的崭新阶段。一份严谨、翔实、具有深刻洞察力的检查后报告,不仅是向监管部门展示机构专业态度与整改能力的关键文件,更是机构将外部审视转化为内部质量跃升的重要载体。其编制质量直接关系到对检查结果的理解深度与后续工作的方向性。一、检查后报告的核心定位与价值检查后报告,通常由检查组出具正式书面意见后,由申请机构(

国家药物临床试验机构(GCP)资质备案现场检查结束后,专家提出的问题与建议并非程序的终点,而是机构质量管理体系迈向更高成熟度的重要契机。对这些反馈进行科学分析、制定有效整改措施并形成闭环管理,不仅是确保备案成功的必要环节,更是机构构建持续改进能力、提升临床研究质量的核心过程。本文将系统阐述检查后的问题分析与应对之道。一、现场检查反馈的性质与分类理解首先需正确理解专家提出问题的性